Chirurgie micro-invasive du glaucome (CMIG) : risques, avantages et pertinence d’utilisation
Related content
Aux stades précoces du glaucome, les dispositifs de chirurgie microinvasive du glaucome (CMIG) peuvent aider à gérer la pression intraoculaire (PIO) et donc réduire la dépendance des patients à l’égard des médicaments. Toutefois, la réduction de la PIO est souvent faible et ces dispositifs sont onéreux.
Au cours des dernières années, la chirurgie microinvasive du glaucome (CMIG) est devenue une option thérapeutique pertinente pour le traitement du glaucome. Si l’on veut enrayer l’évolution de cette maladie, la réduction de la pression intraoculaire (PIO) demeure le seul traitement dont l’efficacité a été démontrée1. Traditionnellement, cette réduction de la PIO est obtenue tant par des interventions non chirurgicales (médicaments topiques ou traitement au laser) que par des interventions chirurgicales (trabéculectomie ou implants de drainage). Aucune de ces méthodes n’est idéale : le manque d’observance thérapeutique est un problème dans le cas du traitement médicamenteux et la chirurgie du glaucome entraîne fréquemment des complications. La CMIG présente un très bon profil d’innocuité ; elle peut donc être mise en oeuvre plus tôt que la chirurgie du glaucome classique dans un plan de prise en charge, et elle est généralement associée à la chirurgie de la cataracte chez les patients présentant un glaucome primaire à angle ouvert (GPAO) léger ou modéré2.
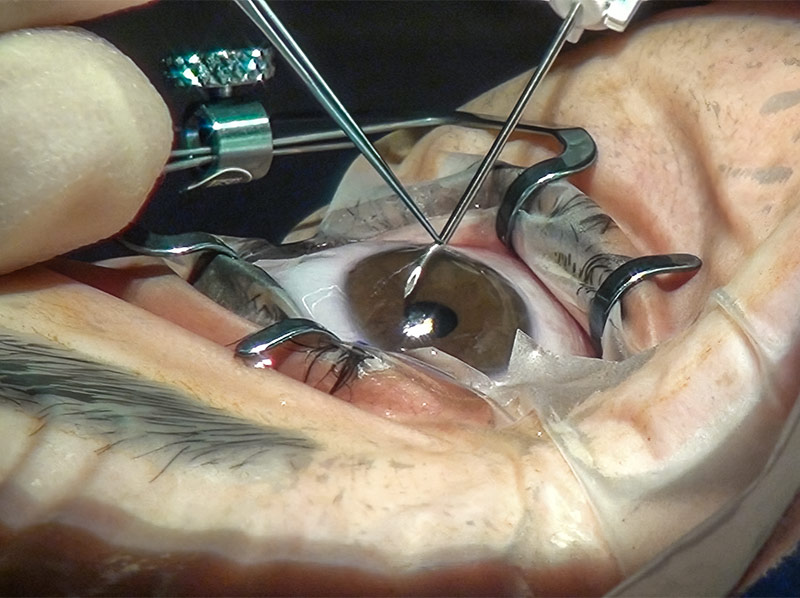
La CMIG consiste à insérer ou placer un petit dispositif par une incision interne en cornée claire. Ceci permet de limiter au maximum le traumatisme tissulaire, d’améliorer le profil d’innocuité et d’accélérer la récupération, par rapport à une trabéculectomie conventionnelle ou un implant de drainage (Figure 1).
L’avantage est que la CMIG est une intervention relativement sûre et peu risquée. Elle n’aboutit toutefois qu’à une réduction de la PIO relativement faible et il n’y a aucune preuve valable pour suggérer que ce type de chirurgie soit d’une quelconque utilité dans un pays à faible ou moyen revenu où le glaucome risque d’être diagnostiqué à un stade très avancé.
À l’heure actuelle, le chirurgien du glaucome a le choix entre un grand nombre de dispositifs de CMIG. Ces dispositifs peuvent être répartis selon leur site d’action ou selon leur localisation : supra-choroïdienne, sous-conjonctivale, ou encore dans le canal de Schlemm.
1. Dispositifs insérés dans le canal de Schlemm Trabectome, ELT (trabéculectomie au laser excimer), iStent, iStent inject, Hydrus, et lame double Kahook (KDB en anglais)
Les dispositifs placés dans le canal de Schlemm sont insérés par une incision interne avec l’aide d’un verre à gonioscopie ; ils visent à augmenter l’écoulement de l’humeur aqueuse par la voie conventionnelle. Par conséquent, leur effet sur l’écoulement de l’humeur aqueuse dépend de la résistance exercée par la pression veineuse épisclérale (Figure 2). Les interventions les plus courantes incluent l’exérèse de tissu trabéculaire (Trabectome, ELT, KDB) ou l’implantation d’un petit dispositif (iStent, iStent inject, Hydrus). Les essais cliniques aléatoires portant sur les dispositifs actuellement disponibles ont montré que le drain Hydrus permettait mieux que le drain iStent de contrôler le glaucome sans médicaments et de diminuer la PIO ; toutefois, l’ampleur de ces effets était faible 3,4.
2. Dispositifs supra-choroïdiens Cypass et iStent Supra
Lorsque l’on utilise des dispositifs placés dans le canal de Schlemm, l’écoulement de l’humeur aqueuse est affecté par la pression veineuse épisclérale. L’espace supra-choroïdien, au contraire, n’exerce qu’une résistance minimale à l’écoulement de l’humeur aqueuse ; cette dernière peut traverser directement la sclère par les espaces intercellulaires entre les fibres du muscle ciliaire et le tissu conjonctif lâche de l’espace supra-choroïdien.

À l’heure actuelle, il n’existe pas de dispositif suprachoroïdien disponible, puisque le micro-stent CyPass (approuvé par la FDA en 2016) a été retiré du marché après qu’une étude post-commercialisation a montré qu’il était associé à une accélération de la perte de cellules endothéliales5. Le iStent Supra est encore à l’essai.
3. Dispositifs sous-conjonctivaux XEN-45 et drain PreserFlo
L’espace sous-conjonctival, bien qu’il ne fasse pas partie du mécanisme physiologique d’écoulement de l’humeur aqueuse, est la voie de drainage que connaissent le mieux les chirurgiens du glaucome car elle est utilisée dans la chirurgie du glaucome traditionnelle. Tout comme l’espace supra-choroïdien, l’espace sous-conjonctival est un site potentiel qui n’est pas limité par la pression veineuse épisclérale ; la fibrose et le tissu cicatriciel peuvent toutefois entraver le drainage de l’humeur aqueuse6.
Le drain XEN-45 Gel Stent est un tube biocompatible et hydrophile à base de gélatine de porc réticulée par le glutaraldéhyde. Il peut être implanté suivant différentes techniques (voie externe ou interne, avec ou sans péritomie conjonctivale).
Le drain PreserFlo Microshunt est posé par voie externe nécessitant une dissection de la conjonctive ; il a malgré tout été classé comme dispositif de CMIG par la FDA (Figure 3).

Ces deux dispositifs entraînent la formation d’une bulle de filtration ; ceci vise à limiter ou prévenir une hypotonie postopératoire significative, mais peut par ailleurs entraîner une fibrose importante et un échec du dispositif. L’utilisation d’anti-métabolites et un traitement anti-inflammatoire intensif après l’intervention peuvent permettre de minimiser ce risque.
Discussion
Les dispositifs placés dans le canal de Schlemm entraînent une diminution globale de la PIO plutôt faible mais ont un bon profil d’innocuité ; ils constituent donc une option thérapeutique bienvenue pour les patients présentant un glaucome léger ou modéré et souhaitant réduire leur prise de médicaments. Il n’existe pas de dispositifs supra-choroïdiens disponibles sur le marché et l’utilisation de ces derniers pourrait par ailleurs être liée à des pics de PIO imprévisibles et une hypotonie. Les dispositifs sous-conjonctivaux peuvent ne pas fonctionner s’il y a fibrose sous-conjonctivale et peuvent entraîner des complications liées à la bulle de filtration.
Lorsque l’on envisage d’utiliser des dispositifs de CMIG dans des régions du monde où les ressources sont limitées en matière de santé, il faut garder à l’esprit les points-clefs suivants : les patients sont susceptibles de présenter un glaucome très avancé et les dispositifs de CMIG seront probablement moins efficaces chez ce groupe de patients ; par ailleurs, les essais thérapeutiques menés à ce jour n’ont porté que sur des personnes présentant un glaucome précoce ou modéré.
La chirurgie du glaucome conventionnelle reste la meilleure technique de prise en charge chirurgicale du glaucome et aucun essai clinique aléatoire n’a comparé directement un dispositif de CMIG et une trabéculectomie ou un implant de drainage de l’humeur aqueuse.
Pour finir, les dispositifs de CMIG sont assez onéreux et ne sont probablement pas une option réaliste dans un pays aux ressources limitées. Certains implants de drainage coûtent à peine 50 dollars US, par rapport à 400 dollars ou plus pour un dispositif de CMIG ; ce prix ne tient d’ailleurs pas compte du coût supplémentaire engendré par l’utilisation de verres de gonioscopie et l’apprentissage intensif nécessaire pour pouvoir réaliser ce type de chirurgie.
La CMIG est un domaine thérapeutique en pleine évolution ; il faudra mener plus d’études de cohortes, avec des périodes de suivi plus longues, pour évaluer plus avant son efficacité et sa sûreté. Il serait également utile de mener des études comparatives supplémentaires pour comparer entre eux différents dispositifs et évaluer leur efficacité relative.
Références
1 Garway-Heath DF, Crabb DP, Bunce C, et al. Latanoprost for open-angle glaucoma (UKGTS): A randomised, multicentre, placebo-controlled trial. Lancet. 2015;385(9975): 1295-1304.
2 Gillmann K, Mansouri K. Minimally invasive glaucoma surgery: Where is the evidence? Asia Pac J Ophthalmol. 2020;9(3):203-214.
3 Otarola F, Virgili G, Shah A, Hu K, Bunce C, Gazzard G. Ab interno trabecular bypass surgery with Schlemm’s canal microstent (Hydrus) for open angle glaucoma. Cochrane Database Syst Rev. 2020;2020(3).
4 Ahmed IIK, Fea A, Au L, et al. A Prospective Randomized Trial Comparing Hydrus and iStent Microinvasive Glaucoma Surgery Implants for Standalone Treatment of Open-Angle Glaucoma: The COMPARE Study. Ophthalmol. 2020;127(1):52-61.
5 Alcon announces voluntary global market withdrawal of CyPass Micro-Stent for surgical glaucoma | Novartis. Accessed August 14, 2021. https://www.novartis.com/news/mediareleases/alcon-announcesvoluntary-global-marketwithdrawal-cypassmicro-stent-surgicalglaucoma 6 Chen DZ, Sng CCA. Safety and Efficacy of Microinvasive Glaucoma Surgery. J Ophthalmol. 2017;2017.

